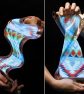
浸大研納米彈簧減藥物副作用
原文刊於信報財經新聞「StartupBeat創科鬥室」

黃陟峰博士透露,新淨化藥物方法現處於概念驗證階段。(浸大圖片)
香港浸會大學物理系研發新的淨化藥物方法,透過轉動設置於納米結構製作儀器內的基板,以宏觀方法控制藥物分子的手性(chirality),從而消除會令藥物出現副作用的手性分子,聲稱能以較低成本生產更純淨及安全的藥物,相關研究已在科學雜誌《自然化學》發表。
浸大物理系副教授黃陟峰博士表示,大部分化學分子均有左、右兩種手性,其原子組成一樣,但空間排列不同,彼此的結構有如鏡像,兩者或具有完全不同的生物化學作用。因此把兩種手性分子分離,或是生產具備治療效果的單一手性分子(即「單一對映體」),有助製造更安全及有療效的藥物。
由於分子極之細小,僅如頭髮直徑的十萬分之一至百萬分之一,難以用肉眼或人手生產「單一對映體」。研究團隊採用一種稱為「大傾斜角物理氣相沉積」的納米材料製造技術,在一塊基板上製造出金屬(例如銀或銅)納米彈簧。當基板以順時針及逆時針方向旋轉時,便會分別製造出左手性及右手性的金屬納米彈簧。
換句話說,基板旋轉的方向決定了金屬納米彈簧的手性,進而決定所生產分子的手性,實現以宏觀方法控制分子手性。

黃陟峰博士指出,基板旋轉的方向,決定了金屬納米彈簧的手性,進而決定所生產分子的手性。(浸大圖片)
團隊以「2-蒽羧酸」(AC)分子進行實驗,發現當AC分子吸附在右手性金屬納米彈簧表面,並暴露於紫外線時,會優先產生右手性分子產物;當AC分子吸附在左手性的金屬納米彈簧表面,同時暴露於紫外線,便會優先形成左手性分子。
料最快三年可投入應用
是次採用了AC分子實驗,黃博士解釋,「蒽」是重要的醫藥中間體,蒽環類藥物亦是一類常用的化療藥物,可用於治療白血病、乳腺癌、子宮癌及淋巴癌等;常用的蒽環類藥物包括阿霉素、柔紅霉素和米托蒽醌等。
黃博士補充,新方法現仍處於概念驗證階段,仍無法滿足「單一對映體」藥物的生產需要,預計需要3至5年的時間,才能正式投入市場應用。至於生產成本,預計與現有藥物相若,甚至可以降低。
支持EJ Tech
如欲投稿、報料,發布新聞稿或採訪通知,按這裏聯絡我們。